De race naar het vaccin heeft mogelijk geen finish

Een vaccin is de enige weg terug naar het normale leven. Wereldleiders, Madonna, de prins van Monaco en de koning van Jordanië hebben samen 7,4 miljard euro neergeteld voor de koortsachtige zoektocht. Minstens tachtig kandidaat-vaccins zijn al in de running. Waar staan we?
1. Welke soorten vaccins zitten in de race en wat zijn voor- en nadelen?
Nooit heeft de mens in minder dan vijf jaar een vaccin ontwikkeld – laat staan in anderhalf jaar, zoals nu wordt gehoopt. Dankzij een meevaller en een paar ‘trucs’ proberen ontwikkelaars nu (heel) veel sneller te gaan.
De meevaller: het nieuwe coronavirus SaRS-CoV-2 lijkt op al gekende coronavirussen die longaandoeningen veroorzaken, zoals SARS-CoV-1 en MERS. Ook die virussen hebben de typische ‘stekels’ of ‘spikes’ aan de buitenkant, waarmee ze zich aan celreceptoren in ons lichaam vasthaken en zo de cellen binnendringen. Dat de ziekteverwekker en dat cruciale ‘spike-eiwit’ bekend zijn, is tijdswinst.
De trucs gaan van de krachten bundelen en zeer veel geld ertegenaan gooien tot bepaalde onderzoeksfases inkorten of zelfs overslaan, zoals het wachten op de eerste academische publicaties. Ook worden de goedkeuringsprocedures versneld, achtereenvolgende onderzoeksfases zoals tests bij een kleine en bij een grote groep worden gecombineerd, en beloftevolle vaccins gaan al in productie nog voor alle tests zijn afgerond.
Wat ook helpt, is op veel paarden tegelijk inzetten. Zo’n tachtig kandidaat-vaccins zijn in de running. Vier verschillende procedés zijn daarbij het meest beloftevol.
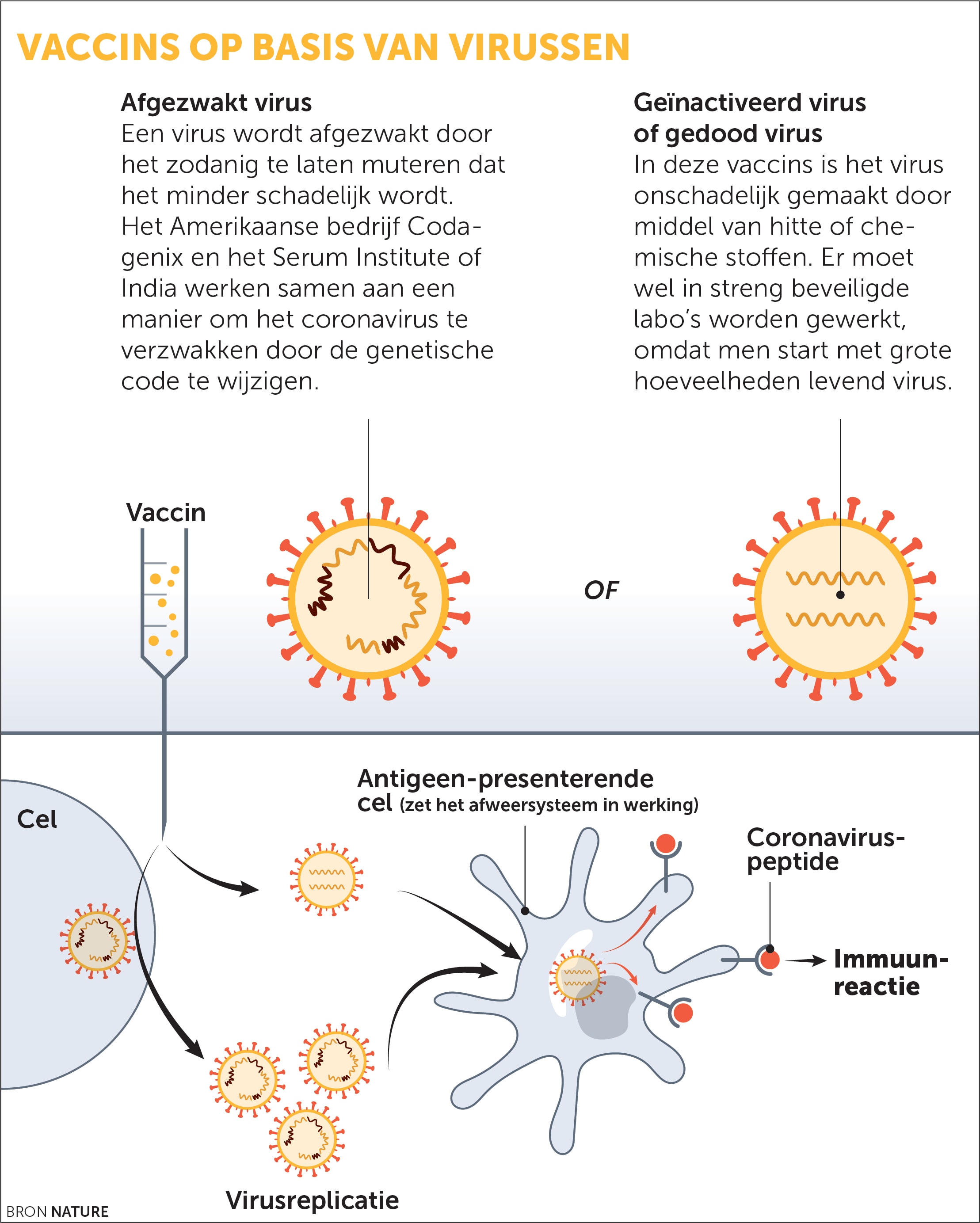
*Geïnactiveerd of gedood virus:
Vaccins op basis van gedood virus zijn allang goed gekend en zijn werkzaam tegen onder andere polio, hepatitis A-virus en seizoensgriep. Het virus wordt door hoge hitte of chemische processen gedood en zo inactief gemaakt. Het vaccin kan je niet ziek maken, maar je lichaam reageert wel op de vreemde indringer door antilichamen aan te maken. Hierdoor is je lichaam beschermd wanneer je het echte virus ontmoet. Om de bescherming nog beter te maken, wordt soms een ‘adjuvans’ aan het vaccin toegevoegd.
De voordelen? Dit procedé is gekend, kan op grote schaal, is eenvoudig en geeft een sterke immuunreactie. Er moet wel in streng beveiligde labo’s worden gewerkt, omdat men start met grote hoeveelheden levend virus.
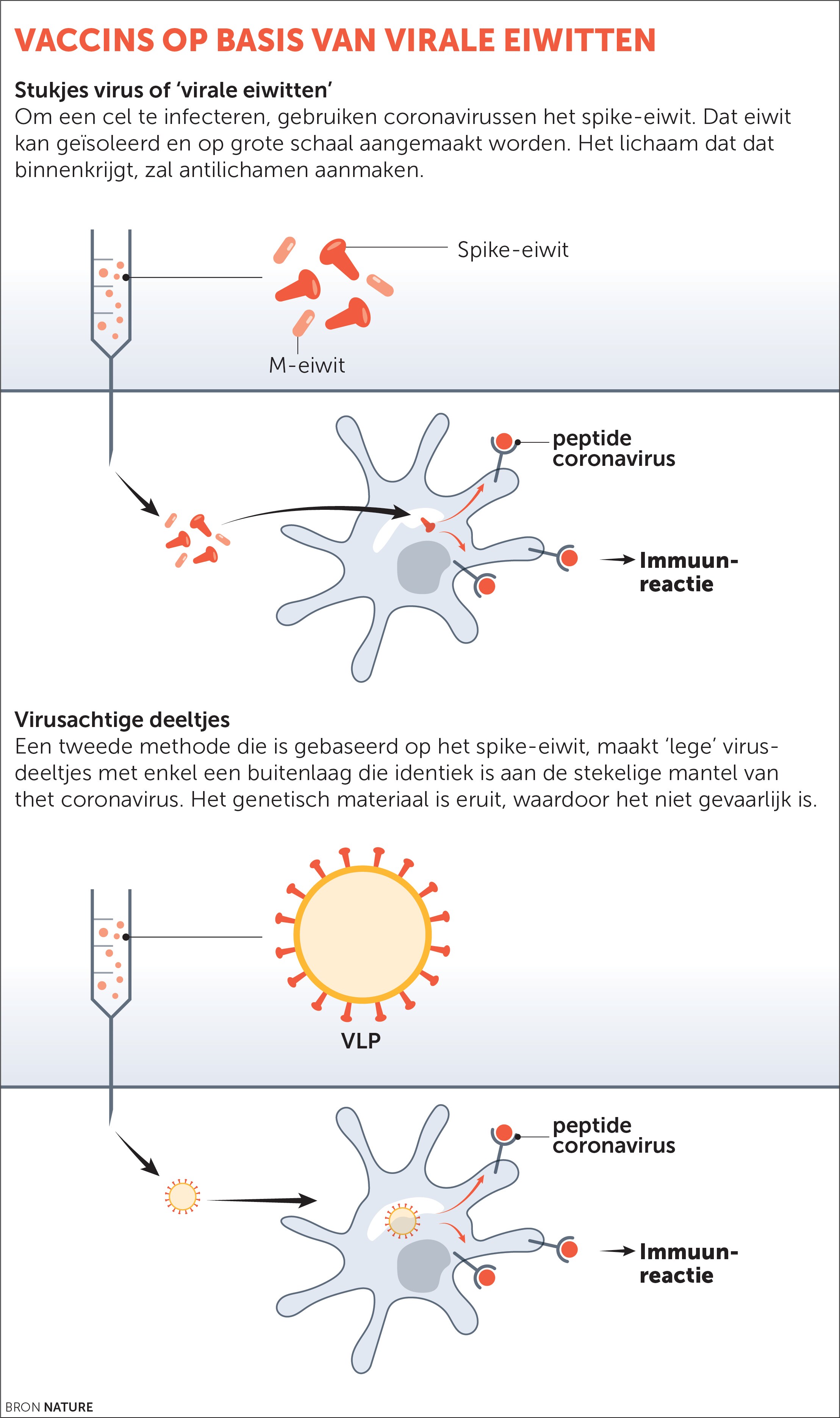
*Stukjes virus of ‘virale eiwitten’:
Om een cel te infecteren, gebruiken coronavirussen het spike-eiwit dat zich bindt aan het celmembraan. Dat karakteristieke eiwit kan geïsoleerd en op grote schaal aangemaakt worden. Een gepaste dosis is dan de basis van een vaccin. Het lichaam dat deze vreemde spike-eiwitten binnenkrijgt, zal antilichamen aanmaken tegen dit cruciale deel van het virus.
Voordeel is dat de techniek bekend is, onder andere van de vaccins tegen hepatitis B en HPV, het humaan papillomavirus. Nadeel is dat veel spike-eiwit aanmaken en zuiveren duur is en dat er doorgaans meerdere dosissen en ook adjuvantia nodig zijn omdat de immuunreactie op een eiwit vaak minder sterk is dan op het volledige virus.
Een tweede methode die is gebaseerd op het spike-eiwit, maakt ‘lege’ virusdeeltjes met enkel een buitenlaag die identiek is aan de stekelige mantel van het coronavirus. Het genetisch materiaal is eruit, waardoor het niet gevaarlijk is. De immuunreactie is sterk en hier zijn doorgaans geen adjuvansen nodig. Deze fopvirussen maken, kan wel moeilijk zijn.
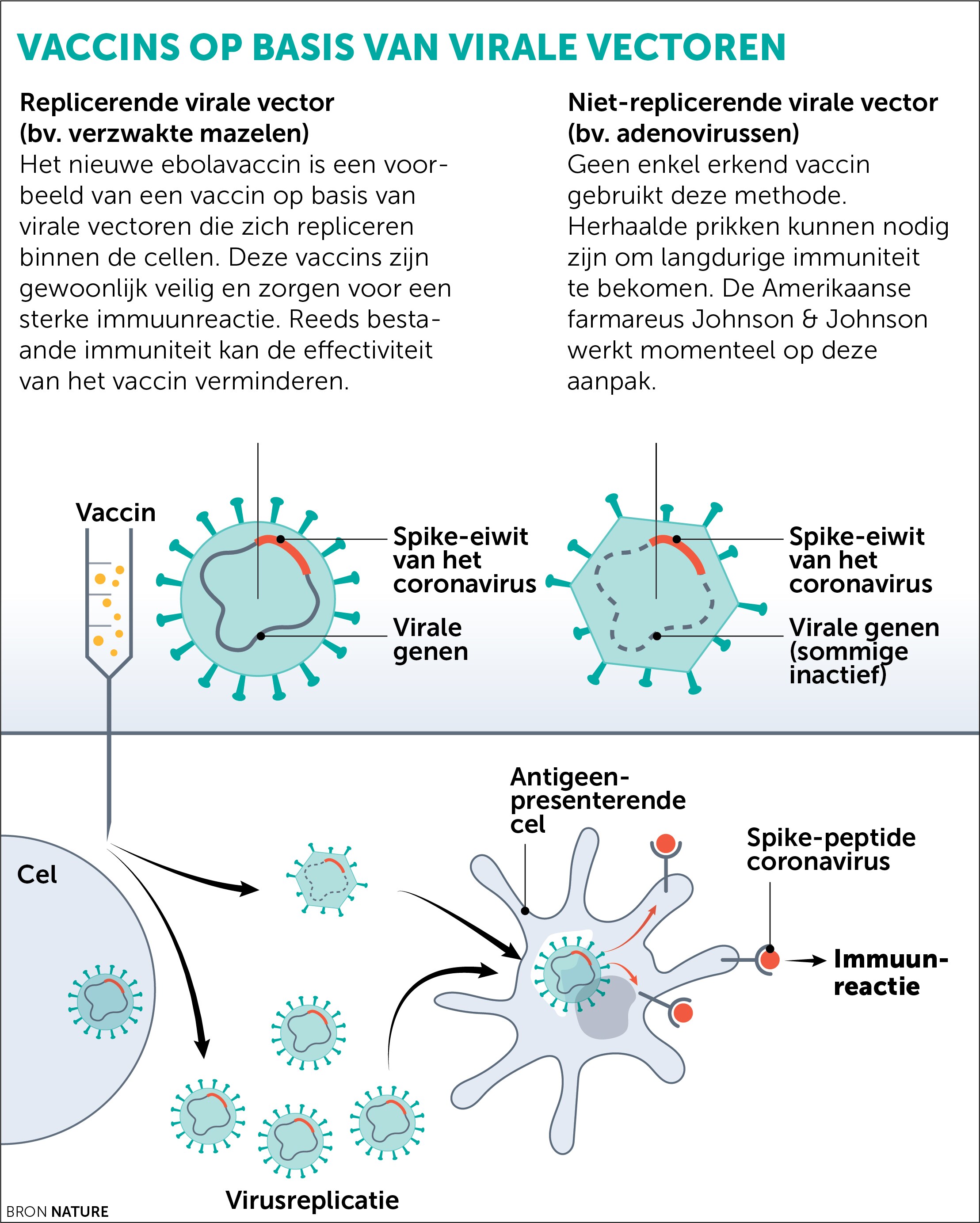
*Virale vector:
Dit type vaccins heet erg veelbelovend in de strijd tegen opkomende infectieziektes en kende succes bij ebola, malaria en MERS, al zijn er nog geen commerciële versies op de markt. Een onschuldig verkoudheids- of mazelenvirus wordt onschadelijk gemaakt en uitgerust met de genetische code voor het spike-eiwit van het coronavirus. De virussen die als koerier dienen, zijn zodanig verzwakt dat ze je niet ziek kunnen maken.
Resultaat: de lichaamscellen waarin die drager-virussen terechtkomen, zullen zelf het spike-eiwit aanmaken. Ons afweersysteem zal dat als vreemd herkennen en het lichaam zal antilichamen aanmaken tegen die rare snuiters.
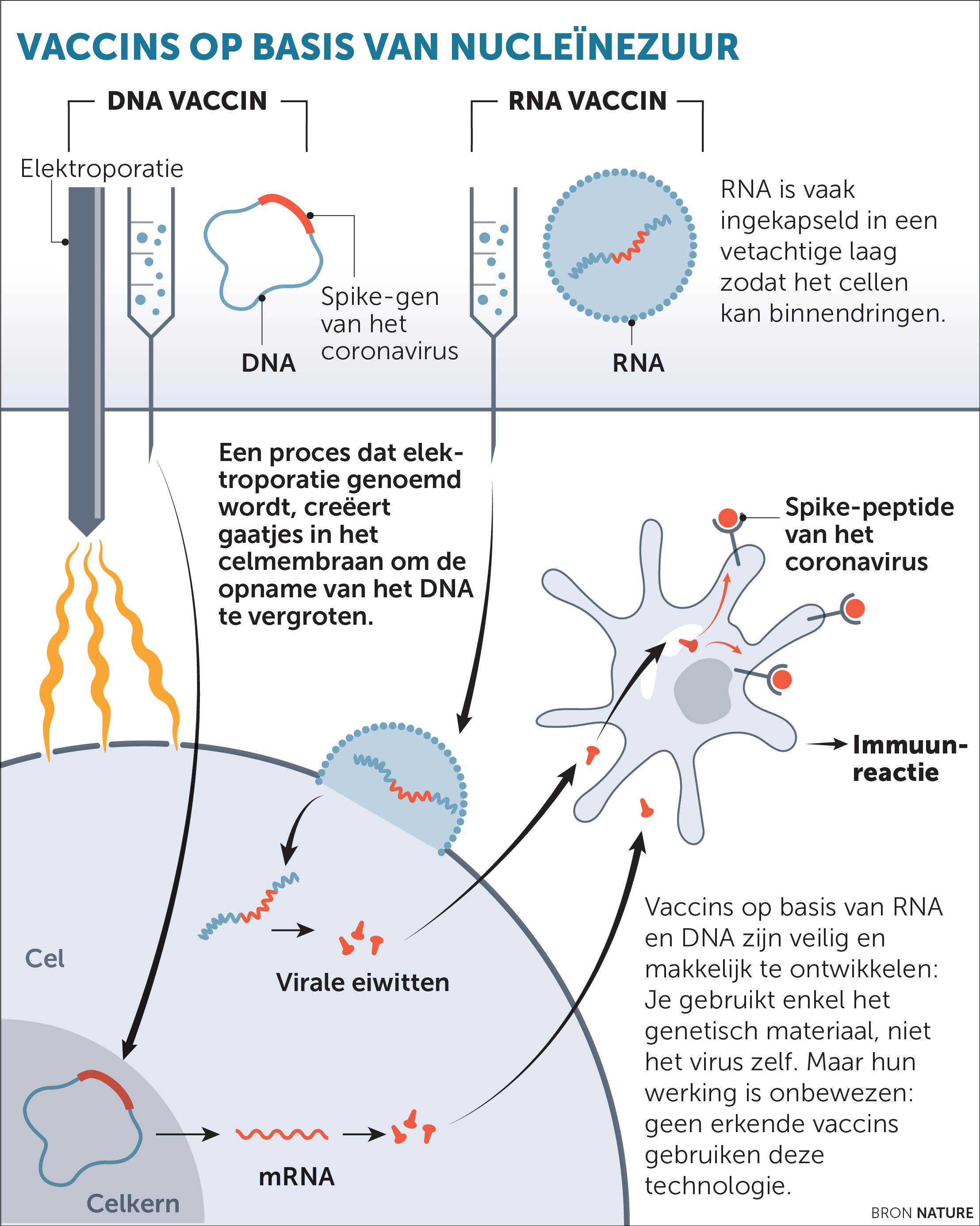
*Nucleïnezuur (DNA, RNA):
Je krijgt geen verzwakt virus of stukje virus ingespoten, maar DNA of RNA dat precies de genetische code om het spike-eiwit aan te maken bevat. Bij een DNA-vaccin wordt die code dan actief in de cellen gebracht. Dat gebeurt meestal mechanisch: door korte elektrische pulsen te geven worden de celwanden even doorlaatbaar, waardoor het DNA-vaccin naar binnen kan. “Het is wel een grote uitdaging om het DNA voldoende in de cellen te krijgen”, zegt professor Isabel Leroux-Roels , diensthoofd van het centrum voor vaccinonologie aan de UGent. “De immuunreactie bij de mens valt vaak tegen.”
‘Boodschapper-RNA’ of ‘mRNA’ speelt een doorslaggevende rol bij de omzetting van DNA in eiwitten. Bij een RNA-vaccin krijg je het stukje mRNA dat codeert voor het spike-eiwit.
Beide methodes maken van eigen cellen kleine fabriekjes van het spike-eiwit. Als reactie daarop ontwikkelt het immuunsysteem antilichamen.
Voordeel is dat er geen problemen zouden mogen optreden met de juiste vorming van het eiwit. Ook zijn hier geen adjuvantia nodig en is dit soort vaccin snel op grote schaal en veilig te maken. Er is enkel de genetische sequentie van het virus nodig om het binnen enkele weken te fabriceren en op te schalen. “De resultaten van mRNA-vaccins zijn wel veelbelovender en geven een veel sterkere immuunreactie dan DNA-vaccins”, zegt Leroux-Roels.
Nadeel is dat dit een totaal nieuwe techniek is en zulke vaccins nog niet op de markt zijn. Ook is de toediening niet zo eenvoudig. Het is bovendien niet zeker dat mensen langdurig beschermd zijn.
2. Wie loopt voorop in de race?
“Het is niet evident om dat objectief te beoordelen, omdat er natuurlijk commerciële belangen meespelen”, zegt immunoloog Joeri Aerts (VUB). “De meest objectieve manier is nagaan wie al met klinische trials bij de mens bezig is.”
Er zijn momenteel een tachtigtal kandidaat-vaccins in ontwikkeling, waarvan minstens zes al in die fase van de klinische testen zitten. Zeventig bevinden zich nog in de preklinische fase met tests bij dieren. Gewoonlijk ligt er een tot twee jaar tussen de preklinische en klinische tests.
Onder de zes koplopers: twee geïnactiveerde vaccins (met of zonder adjuvans), een DNA-vaccin, een mRNA-vaccin en twee vaccins op basis van een virale vector. Meestal is de basis het ‘geraamte’ van een al bestaand vaccin. “Daardoor gaat het sneller, maar het kan ook betekenen dat het dan uiteindelijk niet werkt”, zegt Aerts.
Het kandidaat-vaccin van CanSino Biological / Beijing Institute of Biotechnology lijkt al het verst gevorderd. Fase 2 van de klinische studie is al gestart, waarin men de veiligheid bij een grotere groep testpersonen wil bevestigen. Dit kandidaat-vaccin werkt met een virale vector: een verkoudheidsvirus dat het genetisch recept meekrijgt voor het spike-eiwit. Zo’n 25 andere teams zeggen dat ze hier ook mee bezig zijn, waaronder Janssen Pharmaceutica (Johnson & Johnson), dat in september met de klinische tests start.
Ook het kandidaat-vaccin van de universiteit van Oxford werkt volgens dit procedé en staat ver. “Hun eerste studie combineert meteen fase 1 en 2”, zegt Leroux-Roels. “De autoriteiten hebben toegestaan dat zij fases 1 en 2 combineren omdat zij al ervaring hebben met een vaccin tegen MERS, wat een ander coronavirus is.”
Een derde koploper is het vaccin van het Chinese Sinovac Biotech, dat ook al op mensen test met een kandidaat-vaccin op basis van het meest eenvoudige procedé: geïnactiveerd virus. Minstens zeven andere teams volgen ook deze route. “Maar Sinovac heeft een belangrijke voorsprong omdat ze al ervaring hadden met een SARS-vaccin, het virus dat het meest gelijkt op het huidige SARS-CoV-2 virus”, zegt Leroux-Roels.
Een twintigtal teams zijn aan de slag met DNA of RNA-vaccins. Het verst daarin staan het Amerikaanse Moderna en Inovio en het Duitse BioNTech. Zij zitten ook al in de klinische fase. Ze gebruiken mRNA-vaccintechnologie die ze al ontwikkelden in de context van kankervaccins.
“Om kostbare tijd te winnen, zijn enkele bedrijven zoals Sinovac en Astra Zeneca, in samenwerking met Oxford, ook al op grote schaal vaccins aan het produceren”, zegt Leroux-Roels. “Een risico. Maar lopen de klinische studies goed, dan zullen die vaccins snel beschikbaar zijn.”
3. Hoe realistisch is de timing van anderhalf jaar?
We horen geregeld dat er binnen anderhalf jaar een vaccin zou zijn. Maar sommigen die zelf niet aan de race meedoen, klinken veel pessimistischer. “Een vaccin zal nog jaren op zich laten wachten”, zei de Duitse minister van Volksgezondheid Jens Spahn eergisteren.
“Doorgaans duurt de ontwikkeling dan ook tien à vijftien jaar”, zegt Leroux-Roels. “En dit is een nieuw virus, waartegen nog geen vaccin bestaat.” Bovendien valt een erg grote meerderheid van kandidaat-vaccins af doorheen de vele testfases.
“Enkele bedrijven hadden gelukkig al ervaring met vaccins tegen gelijkaardige virussen zoals SARS en MERS”, zegt Leroux-Roels. “Ook erg belangrijk is dat de regelgevende instanties die de klinische studies en de registratie van het vaccin moeten goedkeuren, hun procedures nu aanpassen om tijd te winnen.”
Kijk je enkel naar de ontwikkeling van het vaccin, dan is anderhalf jaar volgens Aerts een realistische timing, omdat de meesten starten met platformen die al goed gekend en veilig bevonden zijn.
Het grootste struikelblok is volgens hem bewijzen dat een kandidaat-vaccin werkt. “Hoe gaan ze snel bepalen of het ook effectief voldoende bescherming biedt? We weten nog maar weinig over hoe het immuunsysteem omgaat met SARS-CoV-2. Maar het zou veel te veel tijd in beslag nemen om dat eerst te onderzoeken. Daarom is het een beetje nattevingerwerk en extrapolatie van wat wel al bekend is. Om echt heel goed de effectiviteit na te gaan, moet je paradoxaal genoeg hopen dat er nog voldoende besmette mensen zijn, want blootstelling is de enige echte test.”
Ondanks de indrukwekkende bedragen en fonkelende start van enkele kandidaat-vaccins, is het dus niet zeker of er een effectief vaccin komt en al helemaal niet of dat binnen anderhalf jaar zal zijn. En stel dat de wereld dat geluk heeft, dan moeten vervolgens nog razendsnel miljarden dosissen ‘eerlijk’ verdeeld worden. Daarom eist België nu dat het patent op een coronavaccin bij de Wereldgezondheidsorganisatie wordt ondergebracht. De praktische, ethische en geopolitieke hindernissen gaan we in ieder geval niet in een drafje nemen.
Lees ook
Geselecteerd door de redactie


