AstraZeneca onderbreekt proeven met coronavaccin na ‘ongewenste bijwerkingen’ bij proefpersoon

Het Britse farmabedrijf AstraZeneca en de Universiteit van Oxford onderbreken om veiligheidsredenen de vergevorderde proeven met hun potentieel coronavaccin. Het kandidaat-vaccin heeft mogelijk ongewenste bijeffecten veroorzaakt bij een proefpersoon. De Europese Commissie ondertekende met AstraZeneca al een eerste contract voor de aankoop het coronavaccin. Voor België zijn 7,5 miljoen dosissen gereserveerd.
“Standaard beoordelingsprocedures hebben aanleiding gegeven tot een onderbreking van de vaccinaties om de veiligheidsdata te beoordelen”, zegt een woordvoerder van AstraZeneca in een verklaring aan gezondheidsnieuwswebsite Stat News.
Volgens de woordvoerder gaat het om “een routinebesluit”. “Bij grote experimenten komen er altijd toevalligheden voor, maar die moeten nu door een onafhankelijke commissie grondig onderzocht worden”, klinkt het. Ook zegt hij dat het bedrijf “eraan werkt om de beoordeling te bespoedigen om de mogelijke impact op de tijdlijn van de trial te minimaliseren.”
Er mogen geen nieuwe tests uitgevoerd worden, maar de vrijwilligers die al een dosis kregen, worden wel nog verder opgevolgd.
Een ingewijde zegt dat de proeven zijn stilgelegd vanwege “een grote mate van voorzichtigheid". Een tweede ingewijde, die niet met naam en toenaam genoemd wil worden, stelt dat de bevinding die tot de onderbreking heeft geleid, invloed heeft op de toekomstige proeven door AstraZeneca en ook op die van andere farmaceuten.
Lees ook:
De wereldwijde race naar het coronavaccin: de kansen van de acht koplopers op een rij
Ongewenste bijeffecten
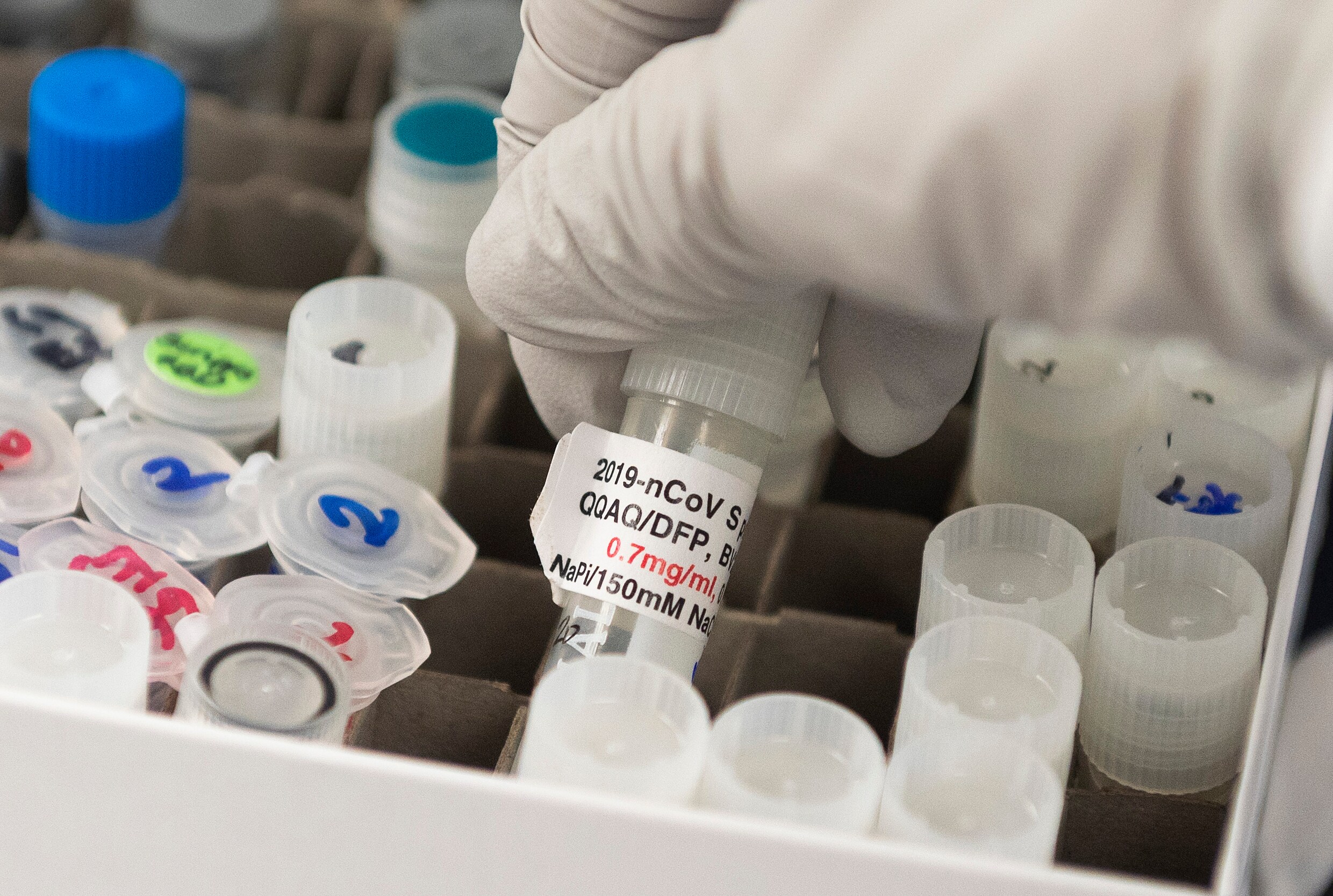
De proeven, die in de derde fase zijn, worden momenteel uitgevoerd in de Verenigde Staten. De proef waarbij de ongewenste bijeffecten zouden zijn opgetreden vond plaats in het Verenigd Koninkrijk. Het is onduidelijk hoelang de onderbreking zal duren. De proefpersoon zou volgens een dichte bron, wel weer volledig moeten herstellen.
AstraZeneca begon eind vorige maand met de proeven en is een van de drie farmaceutische bedrijven die momenteel in een laat stadium testen voor een mogelijk vaccin. De andere twee zijn Pfizer en Moderna, die beiden eind juli met hun trials begonnen.
In juli publiceerde AstraZeneca gegevens waaruit bleek dat het vaccin in een vroeg stadium een veelbelovende immuunrespons opleverde. Het vaccin bleek goed verdragen te worden en er waren geen ernstige bijwerkingen, aldus de onderzoekers destijds. Vermoeidheid en hoofdpijn werden het meest gemeld, zeiden ze. Andere vaak voorkomende bijwerkingen waren pijn op de injectieplaats, spierpijn, koude rillingen en koorts.
Race naar vaccin
Negen grote Amerikaanse en Europese farmaceutische bedrijven, waaronder AstraZeneca, schreven dinsdag nog in een open brief dat ze hun vaccins voor het coronavirus pas op de markt brengen wanneer ze veilig en effectief blijken. Het document is bedoeld om de perceptie tegen te gaan dat er gezondheidsrisico’s worden genomen om maar zo snel mogelijk een coronavaccin op de markt te kunnen brengen. Het vertrouwen van het grote publiek is noodzakelijk omdat een groot deel van de mensen het middel zal moeten gebruiken om het effectief te maken.
De Europese Commissie ondertekende met AstraZeneca al een eerste contract voor de aankoop het coronavaccin. Als het bedrijf erin slaagt het ontwikkelingsproces van zijn vaccin tegen COVID-19 met succes te voltooien, zullen de Europese lidstaten er 300 miljoen dosissen van kunnen aankopen, met een optie voor 100 miljoen extra dosissen. Die zullen worden verdeeld op basis van het aantal inwoners per lidstaat. Voor België zijn 7,5 miljoen dosissen gereserveerd.

Lees ook
Geselecteerd door de redactie